항균제감수성검사, 종류와 새로운 결과보고 방식(디스크 확산법과 최소억제농도 검사법)
항균제감수성검사(antimicrobial susceptibility testing; AST)의 목적은 감염을 일으킨 세균 또는 진균의 성장을 멈추는데 효과적인 특정 항균제를 선택하기 위함입니다. 국내 보험체계에서 인정하는 검사방법은 2가지로 디스크확산법(disk diffusion method)과 최소억제농도검사법(minimum inhibitory concentration; MIC)이 있습니다.
●디스크확산법
디스크확산법은 항균제가 포함된 디스크를 배지에 올려두면 디스크 주위로 항균제 성분이 농도 기울기를 형성하면서 확산하는 원리를 이용합니다. 세균이 항균제감수성을 가질 경우, 항균제 성분이 특정 농도 이상인 부분에서 세균의 생장이 억제되어 고리 모양의 억제 영역을 관찰할 수 있습니다. 검사실에서는 억제 영역의 지름을 측정하여 세균이 항균제에 어느 정도의 감수성을 가지는 지를 판단하게 됩니다.
●최소억제농도검사법
최소억제농도검사법은 항균제의 두배 희석(예: 16, 8, 4, 2, 1, 0.5, 0.25 ug/ml)을 통하여 시각적 또는 자동화된 방법으로 균의 발육을 검출하게 되는데 세균 발육이 완전히 억제되는 가장 낮은 항균제 농도를 포함하는 미량희석액이 MIC로 기록됩니다.
이 방법은 검사실에서 사용하는 가장 보편화된 검사방법으로 우리나라 대부분의 검사실은 상업적으로 공급되는 미량희석배지를 사용하여 최소억제농도를 검사합니다. 자동화된 항균제감수성검사 시스템에는 Vitek 2 system (bioMerieux Inc., Durham, NC), MicroScan WalkAway system (Beckman Coulter Inc., Brea, CA), Phoenix system (BD Microbiology Systems, Sparks, MD) 등이 있습니다.

Fig 2. 최소억제농도검사법을 검사할 수 있는 자동화장비와 카트리지의 예시.
A.Vitek 2 system B. MicroScan WalkAway system C. Phoenix system
●판독기준
Table 1. 판독기준점 예시
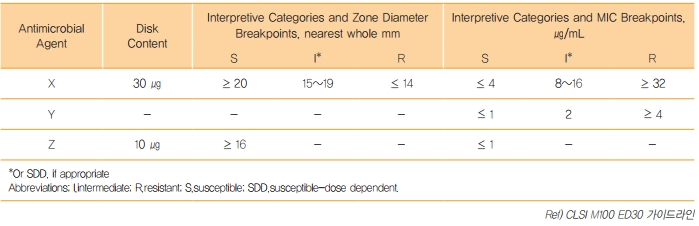
항균제 X는 디스크확산법과 최소억제농도검사법의 판독기준점을 둘 다 가지고 있기 때문에 두가지 방법 모두 검사 및 판정이 가능합니다. 하지만 항균제 Y의 경우에는 MIC 기준만 가지고 있으므로 최소억제농도검사법으로만 검사가 가능하고 디스크확산법으로는 판정을 낼 수 없다. 이는 디스크억제대가 MIC값 관련이 없거나 가이드라인(CLSI M23)에 제시된 대로 평가되지 않았거나 기술적인 문제로 인해 디스크확산법을 사용할 수 없는 경우가 있을 수 있습니다. Z 항균제의 경우는 감수성(S)의 카테고리만 있습니다. 내성 균주가 없거나 드물기 때문에 감수성 이외의 결과 범주를 정의할 수 없는 경우에 해당합니다.
최소억제농도검사법의 장점으로는 정량적인 MIC 검사결과와 함께 판정기준을 알 수 있다는 점이 있습니다. 또한 디스크확산법으로는 검사할 수 없는 일부 무산소성세균이나 배양이 까다로운 세균에 대해서도 정확한 검사가 가능합니다. 특히, CLSI M100 ED30에서는 내세균(non-Enterobacterales)에서 디스크확산법은 충분히 연구가 이루어지지 않았다고 명시하고 있습니다. 또한 Staphylococcus aureus에서의 mecA 유발 oxacillin 내성은 MIC 검사법을 권장한다는 설명이 있다. 때문에 디스크확산법 보다는 최소억제농도검사법으로 검사하는 것을 더 권장한다.
●검사결과 보고
감수성(S; susceptible)은 적정량의 대상항균제를 환자에게 투여하였을 때 감염증이 치료될 가능성이 90% 이상으로 매우 높다는 의미이고 내성(R, resistant)은 치료에 성공할 가능성이 60% 이하로 낮다는 의미입니다. 중간(I; intermediate)은 여러가지 의미가 있는데 고농도로 투여해도 안전한 항균제인 경우 고농도로 투여하면 효과가 있다는 의미일 수도 있고 요로감염과 같이 정상적으로 항균제가 농축되는 부위의 감염 시에는 효과가 있다는 의미일 수도 있습니다.
반대로 뇌척수액과 같이 약물 침투가 어려운 부위의 감염인 경우에는 해당 항균제의 사용을 자제해야 한다는 의미가 되기도 하며 경계에 있는 감수성 결과가 내성으로 잘못 보고되는 것을 막기위한 완충지대를 의미하기도 합니다.
최근 항균제감수성 결과보고에서 SDD (susceptible-dose dependent)라는 카테고리가 새로 생겼습니다. 이것은 환자에서 사용되는 항균제 농도에 중점을 두어 감수성이 될 수 있는 경우를 말하며 균주가 SDD 카테고리에 해당하는 경우, 투약요법을 변경 (고용량 혹은 투약 회수 추가)하면 임상적으로 효과를 볼 수 있다는 점이 입증되었을 때 사용합니다.
항균제 농도가 높을수록 SDD 균주를 커버할 가능성이 높아지므로 SDD가 나온 경우에는 문헌에서 제안하는 최대 투약 용량을 고려하는 것을 권장합니다. 쉽게 말하면, 중간(intermediate)으로 보고되어야 하는 항균제 중에서 투약요법을 고용량 혹은 투약 회수 추가로 변경하는 것이 임상적으로 입증된 항균제의 경우에 SDD로 보고하게 되며 기존 S/I/R 로 보고되던 것을 S/SDD/R로 보고하도록 권고하고 있습니다. CLSI M100-ED30에 따르면, 다음과 같은 균주와 항균제에서는 Intermediate 대신 SDD로 보고하도록 권고하고 있으며 투여약물 용량도 함께 제시하고 있습니다.
Table 2. 균 및 항균제에 따른 SDD 시 투약 용량
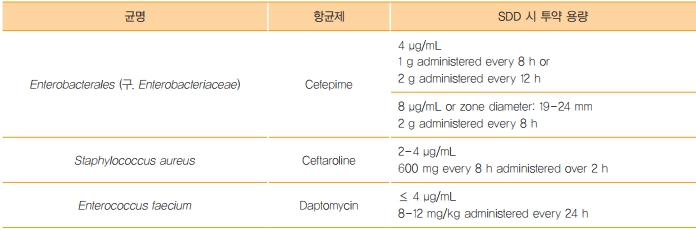
항균제감수성 결과보고에서 I^ 라는 카테고리도 새로 생겼습니다. 이는 소변과 같이 항균제가 농축될 수 있는 부위에서 치료 효과가 있는 경우에 보고하도록 되어있습니다. Enterobacterales 중에서 β-lactam, aminoglycosides, fluoroquinolones과 같은 항균제에서 위와 같은 카테고리를 사용하게 되었고 기존 S/I/R을 S/I^/R로 보고하도록 권고하고 있습니다.
GC녹십자의료재단의 검사실에서는 아직 현재 기준을 적용하지 않고 있는데 SDD와 I^ 둘다 새로운 개념으로 교육이 먼저 선행되어야 할 것으로 생각되기 때문입니다. 특히 I^는 잠정적인 개념으로 내년에 더 명확하게 제시될 예정이므로 GC녹십자의료재단의 검사결과지에는 추후에 반영할 예정입니다.

