GC녹십자의료재단 진단검사의학본부 전문의 안선현
전체 치매 중, 알츠하이머치매가 약 71.3%로 가장 많은 부분을 차지하고, 혈관성치매 16.9%, 기타 치매 11.8% 비율을 차지 하고 있는 것으로 보고되었습니다. 치매가 의심될 경우에는 보호자와 환자 본인의 문진을 통해 인지 또는 행동수행 능력 등을 평가하고, 뇌영상진단(MRI, PET 등)을 활용해 뇌혈관질환 여부 및 뇌위축(brain atrophy) 등을 조사하여 진단이 이루어집니다.
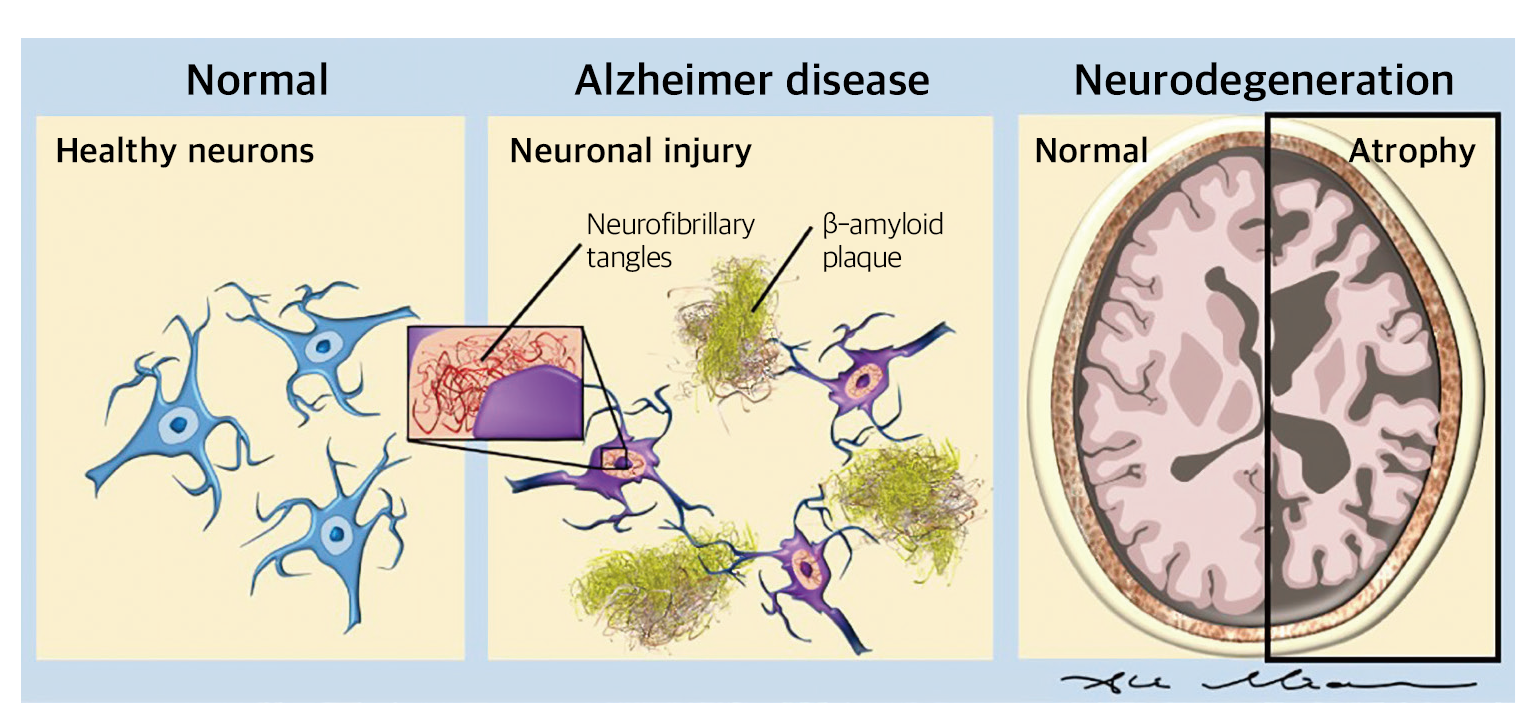
Ref) ALZ imaging-AD pathology and biomarkers
알츠하이머치매는 신경세포 밖에 베타아밀로이드(β-amyloid)가 침착된 아밀로이드플라그(amyloid plaque)와 세포 내에 과인산화된 타우(hyperphosphorylated tau, p-tau)단백질이 축적되어 뇌신경세포(neurons)가 사멸되는 질환입니다.
현재 알츠하이머치매의 치료는 치매를 초기에 발견하여 대증적 치료와 운동 등의 건강관리를 통해 증상을 완화시키고 진행을 지연시키는 것을 목표로 하고 있습니다. 그러나, 뇌영상검사법은 뇌위축이 상당히 진행된 상태에서만 확인이 가능하기 때문에 치매 조기진단을 가능하게 하는 검사법에 대해 많은 연구가 이어지고 있습니다. 따라서, 이 단원에서는 현재까지 알려진 혈액 이나 뇌척수액으로 시행할 수 있는 다양한 알츠하이머병 관련 검사들을 살펴보고자 합니다.
뇌척수액 알츠하이머병 표지자(β-amyloid 1-42, p-tau, p-tau/Aβ42 ratio) [ECLIA]
치매 환자에서 신경퇴화가 진행됨에 따라 베타아밀로이드가 축적되고 아밀로이드플라그가 형성되지만 뇌척수액에서는 베타 아밀로이드 농도 감소가 관찰됩니다. 또한, 신경섬유다발(neurofibrillary tangle)과 관련 있는 타우단백질은 치매 환자의 뇌척수액 에서 전체 타우단백질과 과인산화된 타우단백질 모두 농도가 증가되는 것으로 보고되고 있습니다. 이는 치매 환자에서 뇌신경 세포 사멸에 따라 세포 밖으로 흘러나온 타우단백질이 뇌척수액에서 증가하기 때문인 것으로 보고 있습니다. 이를 활용한 검사법이 각각 CSF-Aβ 및 CSF-tau/p-tau 양을 측정하는 방법입니다. 현재 정상인과 치매 환자 뇌척수액에서 베타아밀로이드 및 타우단백질 평균 농도까지 알려져 있어 이를 이용한 치매 진단 표지자로 개발이 가장 활발한 분야라고 볼 수 있습니다.
p-tau/Aβ42 ratio CSF 분석은 amyloid PET과 약 90% 일치함을 입증함으로써 알츠하이머병 진단에서 PET에 대해 대안이 될 수 있을 것으로 예상하고 있습니다. 그러나, 뇌척수액을 이용한 치매 진단은 요추천자(lumbar puncture)를 통해 뇌척수액을 얻어야 하는 침습적인 방법이라는 문제점이 있습니다.
Table 1. 뇌척수액 알츠하이머병 표지자 2종의 참고범위
검사항목 | 참고치 |
|---|---|
p-tau/Abeta42 ratio | ≤ 0.023 |
β-amyloid (1-42) (Abeta42) | > 1030 pg/mL |
Phospho-tau (181P) (p-tau) | ≤ 27 pg/mL |
Oligomerized amyloid β [ECLIA]
알츠하이머병 의심 환자의 혈장(heparin)에서 베타아밀로이드 올리고머를 전기화학발광면역법(electrochemiluminesc ence immunoassay, ECLIA)으로 정량적으로 측정하는 검사법입니다. 베타아밀로이드는 아밀로이드전구체(amyloi d precursor protein, APP)로부터 가용성인 베타아밀로이드 모노머(Aβ monomer), 다이머(dimer), 올리고머(oligomer), 피브릴(fibril)을 형성하면서 최종적으로는 불용성 플라그를 형성하게 됩니다. 베타아밀로이드 모노머는 세포독성이 없고 정상인에서도 발견되기 때문에, 독성을 갖는 올리고머만을 선택적으로 검출하기 위해 sandwich ELISA를 응용해서 항원에 반응하는 포획/검출 항체의 항원인식부위를 겹치도록 구성한 분석법을 사용합니다.

Fig. 2. 올리고머화 아밀로이드베타 검사의 참고범위
Human amyloid β [ELISA]
알츠하이머병의 베타아밀로이드 40 또는 42개의 아미노산으로 구성된 펩타이드로, 플라그는 주로 Aβ1-42, 그 외에 Aβ1-40, Aβ4-38 등이 침착되는 것으로 알려져 있습니다. 또한 많은 연구에서 알츠하이머 환자의 뇌척수액 및 혈액 내 Aβ1-40 농도의 증가, Aβ1-42 농도의 감소 또는 경도 증가를 보고하고 있으며 그 결과 Aβ1-42/Aβ1-40의 비율은 감소 하는 것으로 알려져 있습니다. 이러한 다양한 크기의 베타아밀로이드의 농도를 효소결합면역흡착법(enzyme-linked immunosorbent assay)으로 측정하는 검사입니다.
Table 2. Human amyloid β 검사의 참고범위
단위 : pg/mL
성별 | Aβ1-40 | Aβ1-42 | 42/40 ratio |
남성 | 128.38~297.44 | 2.13~12.64 | 0.010~0.080 |
여성 | 125.38~332.23 | 2.50~22.16 | 0.010~0.110 |
APOE (apolipoprotein E) genotype [Real-time PCR]
APOE는 주로 간에서 생성되는 아포지단백질로, 중추신경계에서는 콜레스테롤을 신경세포로 수송합니다. APOE 유전자는 19번 염색체에 위치하고 다형성으로 E2, E3, E4 (APOE e2, APOE e3, APOE e4) 등 3가지 대립유전자를 갖습니다.
E4는 특히 초저밀도지단백질(very low density lipoprotein, VLDL)에 결합하며 지질 수송, 포도당 대사 및 뇌혈관 기능, 타우 매개 신경변성 과정에도 관여하여, 알츠하이머병 등 다양한 뇌혈관 신경계질환과의 관련성을 갖는다고 보고되고 있습니다. 그러나, 알츠하이머치매는 여러 유전자가 관여하며 환경요인도 작용하므로, 특정 APOE 유전형이 있어도 질환이 발병하지 않을 수 있기 때문에 증상이 있는 환자의 진단 보조 검사로 이용할 수 있습니다.
Table 3. APOE 유전자 검사의 결과 예시
Alzheimer disease | 저위험군 | 중위험군 | 고위험군 | |||
ApoE 유전형 | E2/E2 | E2/E3 | E3/E3 | E2/E4 | E3/E4 | E4/E4 |
|
| ○ |
|
|
| |
알츠하이머병은 인지기능의 저하와 함께 일상생활에 어려움을 초래하기에 환자와 더불어 가족 전체의 삶에 영향을 끼칩니다. 이러한 치매가 조기에 발견되어 진행을 늦출 수 있도록 돕기 위해 다양한 검사법이 알려져 있습니다. 또한, 우리나라 뿐만 아니라 전세계적으로 알츠하이머병의 치료제 연구와 조기 진단법 개발을 위해 지속적으로 노력하고 있기에 민감도와 특이도가 더욱 개선된 검사법들이 앞으로도 꾸준히 개발될 것으로 기대됩니다.
참고문헌
01. Querfurth HW and LaFerla FM. Alzheimer's disease. Engl J Med. 2010 Jan 28;362(4):329-44.
02. Barbara J Snider, Anne M Fagan, Catherine Roe, Aarti R Shah, Elizabeth A Grant, Cheng jie Xiong, et al.
Cerebrospinalfluid biomarkers and rate of cognitive decline in very mild dementia
of the Alzheimer type. Arch Neurol. 2009;66(5):638-645.
03. 보건복지부, 신의료기술평가위원회. 신의료기술평가보고서 HTA-2020-27 올리고머화 베타아밀로이드
[효소결합면역흡착법]. 2020.
04. Saido T.C., Iwatsubo T., Mann D.M.A., Shimada H., Ihara Y., Kawashima S. Dominant and differential deposition of distinct β-amyloid peptidespecies, AβN3(pE), in senile plaques. Neuron.1995 Feb;14(2):457-66.
05. Yu Yamazaki, Na Zhao, Thomas R Caulfield, Chia-Chen Liu, Guojun Bu. Apolipoprotein Eand Alzheimer disease:
pathobiology and targeting strategies. Nat Rev Neurol. 2019 Sep;15(9):501-518.
검사항목 안내
검사항목 | 검체(mL) | 검사일 / 소요일 | 검사방법 | 보험정보 | 결과보고 형식 |
알츠하이머질환 표지자 검사(2종) | CSF 2.5 | 수 / 1일 | ECLIA | 노12 / BZ012 | 별지 결과지 |
Oligomerized amyloid β | Heparin P 3.0 | 월,수 / 3일 | ECLIA | 노117 / CZ117 | |
Human amyloid β | EDTA P 0.5 | 화,목 / 2일 | EIA | - | |
APOE genotype [Real-time PCR] | EDTA WB 3.0 | 월-금 / 3일 | PCR with | 나580나 / |

