GC녹십자의료재단 진단검사의학본부 전문의 박미정, 박찬정
검사의 의의
1. 미세잔존질환의 정의
미세잔존질환(minimal residual disease, MRD)은 암환자에서 치료 후 남아 있는 아주 적은 수의 암세포를 지칭하는 용어입니다. 급성림프모구백혈병(acute lymphoblastic leukemia, ALL)과 다발골수종(multiple myeloma, MM=plasma cell myeloma, PCM) 등의 혈액암 환자에서 치료 후 완전관해(complete remission)/완전반응(complete response)으로 골수의 현미경 판독상 백혈병과 골수종 세포가 관찰되지 않거나 림프모구와 형질세포가 정상 범위일 때, 아주 적은 비율로 혈액암 세포가 남아있을 수 있습니다.
이러한 MRD의 존재 여부는 치료효과의 판정, 환자의 예후 예측, 암 재발의 발견, 최적의 항암치료 적용, 새로운 항암제와 치료 프로토콜 등을 평가하는 데 이용됩니다. 림프모구백혈병 환자에서 미세잔존질환 검사를 시행하는 시기는 치료 단계 또는 방법에 따라 다음 여섯가지로 나눌 수 있습니다.
- 관해유도 중(8일 말초혈액) | - 치료과정 중 필요하다고 판단될 때 - 조혈모세포 이식 전후 |
2. MRD 측정 방법
MRD는 기존의 혈액암 진단에 이용되어 온 형태학적 진단, 혈청에서 단클론단백 등의 검출로는 측정되기 어려우며, 유세포검사(flow cytometry), 중합효소연쇄반응(polymerase chain reaction, PCR), 차세대염기서열분석(next-generation sequencing, NGS) 등의 민감도가 높은 검사법으로 측정합니다. 각 검사법은 장단점이 있으며, 일반적으로는 더 빠르고 검출 민감도가 높은 검사법이 유용하지만, 혈액암의 진단 시 면역표현형과 분자유전학적 특징에 따라 더 효과적인 검사법이 있을 수 있으며, 각 검사법은 상호 보완적으로 사용되고 시행한 모든 검사의 결과를 종합적으로 판단하여야 합니다.
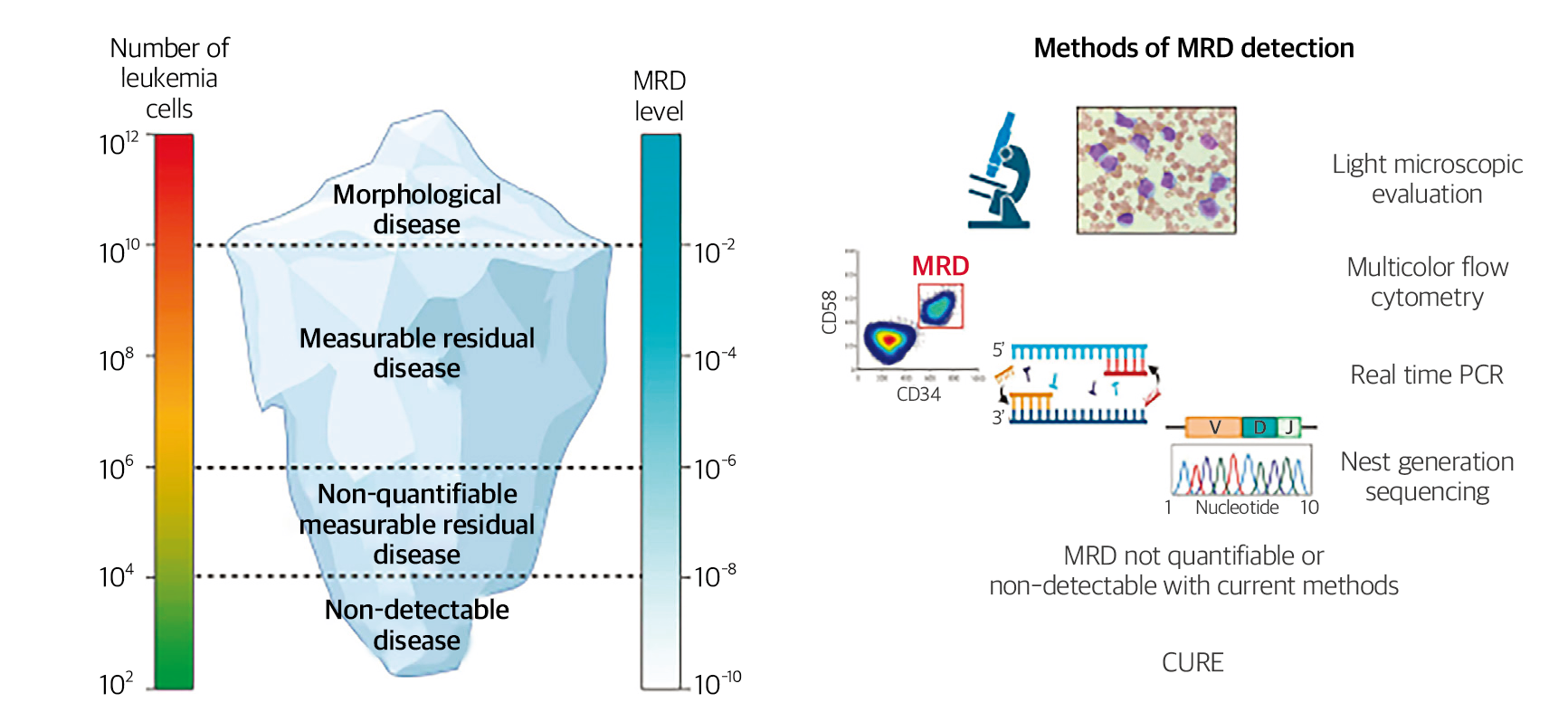
Ref) Haematologica. 2022;107:2783-2793.
Fig. 1. 림프모구백혈병 환자에서 백혈병세포의 양과 미세잔존질환의 양, 백혈병 검사법과 검출 민감도
3. MRD 측정을 위한 유세포검사
환자의 말초혈액, 골수흡인 검체로 시행하며, 세포표면의 면역표현형을 측정하여 혈액암세포를 측정하게 되며, B-ALL의 경우 정상적으로 보일 수 있는 미성숙 B세포(immature B-cell precursors, hematogones)와 감별하여야 하고, 다발골수종의 경우 정상 형질세포와 감별하여야 합니다. MRD 유세포검사는 다른 MRD 검사법과 비교하여 결과 확인이 빠르고, 비교적 경제적 이며, 정상세포에 대한 정보도 확인할 수 있다는 장점이 있습니다.
검사의 원리
유세포분석기(flow cytometer, FCM)는 단일세포 부유액(single cell suspension)이 흐르게 하여 광원(laser)의 빛과 세포(또는 입자)가 부딪친 후 빛의 산란, 형광물질의 발광 현상을 이용하여 세포에 관한 여러 가지 정보를 측정하고 경우에 따라 특정 세포만을 선택하여 분리할 수 있는 장비입니다. 세포표면, 세포질, 핵 내의 항원단백질에 결합하는 항체-형광물질을 결합 시켜서 특정 세포군의 항원발현을 알아낼 수 있고, 세포군의 구별, 원하는 세포의 비율 측정 등에 이용됩니다. 미세잔존질환 검사는 이러한 유세포분석기를 이용하여 말초혈액이나 골수검체에서 아주 적은 비율의 혈액암세포(0.01~0.001%)를 민감한 방법으로 검출하며, 아주 많은 세포에서 적절한 표지자를 이용하여 정상세포와 구별하여 혈액암세포의 존재를 검출합니다.
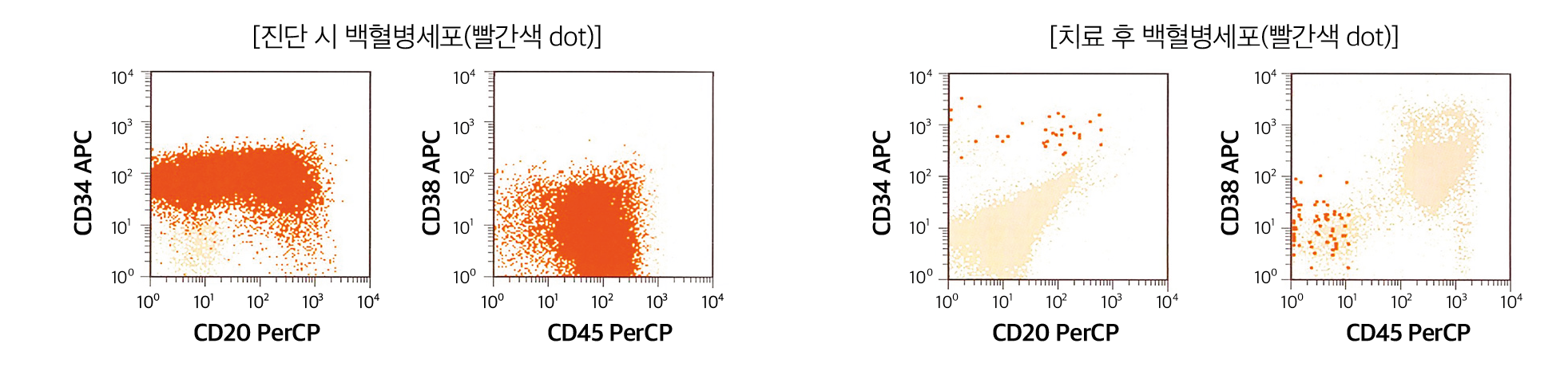
Ref) Flow cytometry in clinical diagnosis/4th edition/ASCP press
Fig. 2. 진단 시와 추적관찰 시 유세포검사에서 측정되는 백혈병세포의 점도표(dot plot) 예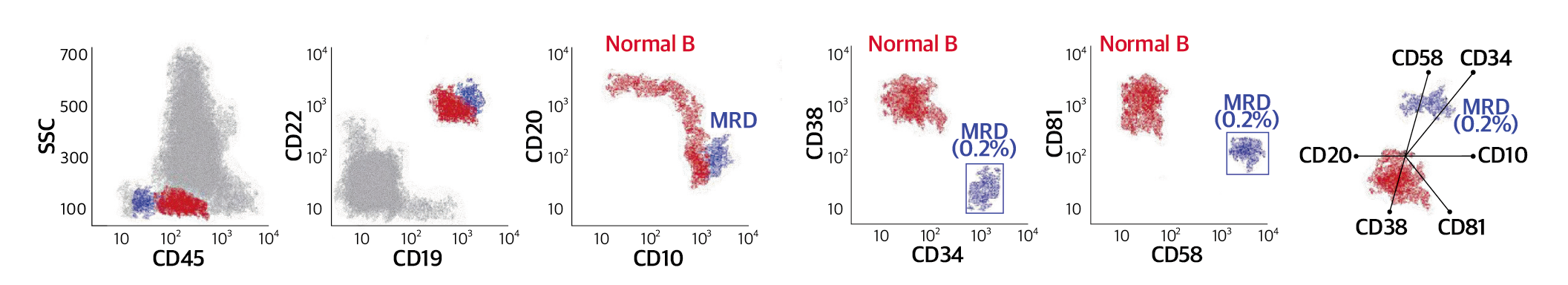
Ref) Haematologica. 2022;107:2783-2793.
Fig. 3. B-ALL에서 유세포검사를 이용한 정상 미성숙 B세포(immature B-cell precursors, hematogones) (빨강 점)와 백혈병세포(MRD) (파란 점)의 감별
위의 세 번째 CD10/CD20 점도표에서는 정상 B세포의 분화/성숙 단계에 따른 성숙경로(maturation pathway)에서 벗어난 것 으로 MRD 백별병세포가 구별됩니다. 정상세포와 백혈병 MRD세포의 감별 전략으로는 진단 시 또는 재발 시 백혈병의 면역 표현형을 확인하고(양, 음성, 형광강도), 그와 같은 MRD 세포군을 확인합니다. 정상세포와 감별할 수 있는 백혈병세포의 이상 항원발현과 백혈병세포의 감별 전략은 다음과 같은 경우가 있습니다.
- 백혈병세포의 계통에서는 발현되지 않는, 다른 세포에서 발현되는 항원의 발현(cross-lineage antigen expression (dim/partial)) - 정상세포에서 분화되는 단계에 따라 발현시기가 다른 항원의 동시발현(asynchronous antigen expression) |
상기 특징을 토대로 B-ALL의 경우 정상 미성숙 B세포와 감별되는 항원들이 있으며, CD10/CD20 등 도표에서 정상 성숙경로 에서 벗어난 백혈병세포(MRD)를 감별할 수 있습니다(Fig. 3). 다발골수종의 경우 형질세포 표면항원의 변화를 측정하여 정상 형질세포와 감별할 수 있습니다. 림프모구백혈병(ALL) 환자에서는 1x10-4 (0.01%), 다발골수종에서는 1x10-5 (0.001%)의 혈액 암세포를 유세포검사로 검출할 수 있습니다. 검사의 정확성을 위해서는 검체의 상태가 중요하며, 골수검체의 경우 말초혈액 으로 희석(hemodilution)되는 것을 막기 위해 골수흡인 검체 채취 시 세포형태 검사용으로 처음 채취하는 골수흡인액을 최소한 (200~500 micL) 채취 후, 바로 MRD 유세포검사용 골수흡인액 1~2.5 mL를 채취하고, 그 후에 다른 검사용 검체를 채취합니다.
결과 해석
림프모구백혈병 환자에서는 1x10-4 (0.01%) 미만, 다발골수종에서는 1x10-5 (0.001%) 미만에서 MRD 음성으로 판단합니다. B-ALL에서는 MRD 음성(< 0.01%), 0.01%≤< 0.1%, 0.1%≤< 1.0%, 1.0%<의 범위로 나누어 볼 때 환자의 생존율에 유의한 차이가 있음이 보고되었고, 국제가이드라인(NCCN Guidelines)에 따르면 진단 8일의 말초혈액에 MRD< 1%, 진단 29일 (관해유도치료 종결) 골수의 MRD< 0.01%인지 확인하여 위험도 평가 및 치료 프로토콜 결정에 이용합니다.
따라서 B-ALL에서는 잔여 MRD세포 양이 해당하는 범위를 확인하고, 치료 과정 중 MRD 지속(치료 중 2회 이상 검사에서 양성)인지 MRD 재발(치료과정 중 음성으로 유지되던 MRD가 양성을 보임)인지 확인함으로써 환자의 치료 추적관찰 및 치료방침 결정에 이용합니다. 다발골수종에서는 MRD< 0.001% 미만을 MRD 음성으로 보고하며, 환자의 치료효과 판정과 질병의 추적관찰, MRD 재발확인과 치료방침 결정에 이용되고 있습니다.
참고문헌
01. Caner Saygin, Joseph Cannova, Wendy Stock, Lori Muffly. Measurable residual disease in acute lymphoblastic
leukemia: methods and clinical context in adult patients. Haematologica. 2022;107:2783-2793.
02. Flow cytometry in clinical diagnosis/4th edition/ASCP press
03. Donald A Berry, Shouhao Zhou, Howard Higley, Lata Mukundan, Shuangshuang Fu, Gregory H Reaman, et al.
Association of Minimal Residual Disease With Clinical Outcome in Pediatric and Adult Acute Lymphoblastic
Leukemia: A Meta-analysis. JAMA Oncol. 2017;13:e170580.
04. Neha Korde, Mark Roschewski, Adriana Zingone, Mary Kwok, Elisabet E Manasanch, Manisha Bhutani, et al.
Treatment With Carfilzomib-Lenalidomide-Dexamethasone With Lenalidomide Extension in Patients With Smoldering
or Newly Diagnosed Multiple Myeloma. JAMA Oncol. 2015;1:746-54.
05. NCCN Guidelines Pediatric Acute Lymphoblastic Leukemia Version 3.2024
06. NCCN Guidelines Acute Lymphoblastic Leukemia Version 3.2023
07. NCCN Guidelines Multiple Myeloma Version 2.2024
08. Alejandro Medina-Herrera, María Eugenia Sarasquete, Cristina Jiménez, Noemí Puig, Ramón García-Sanz. Minimal Residual Disease
in Multiple Myeloma: Past, Present, and Future. Cancers (Basel). 2023;15:3687.
검사항목 안내
검사항목 | 검체(mL) | 검사일 / 소요일 | 검사방법 | 보험정보 |
Acute lymphoblastic leukemia MRD (8종) | EDTA BM 1.0 | 월-금 / 3일 | Flow cytometry | 노12 / BZ012 |
MM-MRD/follow-up immunophenotyping (5종) | EDTA BM 2.0 | 노117 / CZ117 | ||
Plasma cell myeloma immunophenotyping (8종) | EDTA BM 2.0 | - |

